
【코코타임즈】 동물용의약품을 제조 또는 수입하려면 반드시 거쳐야 할 임상•비임상 시험의 실시기관으로 전국 15곳이 최종 선정됐다. 정부가 동물용의약품 인허가를 내주기 위한 심사를 통과하자면 이들 15곳의 시험 결과서를 의무적으로 첨부해야 하는 것이다.
농림축산검역본부(본부장 박봉균, 이하‘검역본부’)는 '동물용의약품등 안전성·유효성 심사에 관한 규정' 개정안이 이달 15일부터 시행됨에 따라 그동안 동물용의약품 등 임상·비임상 시험실시기관 선정작업을 벌여왔다.
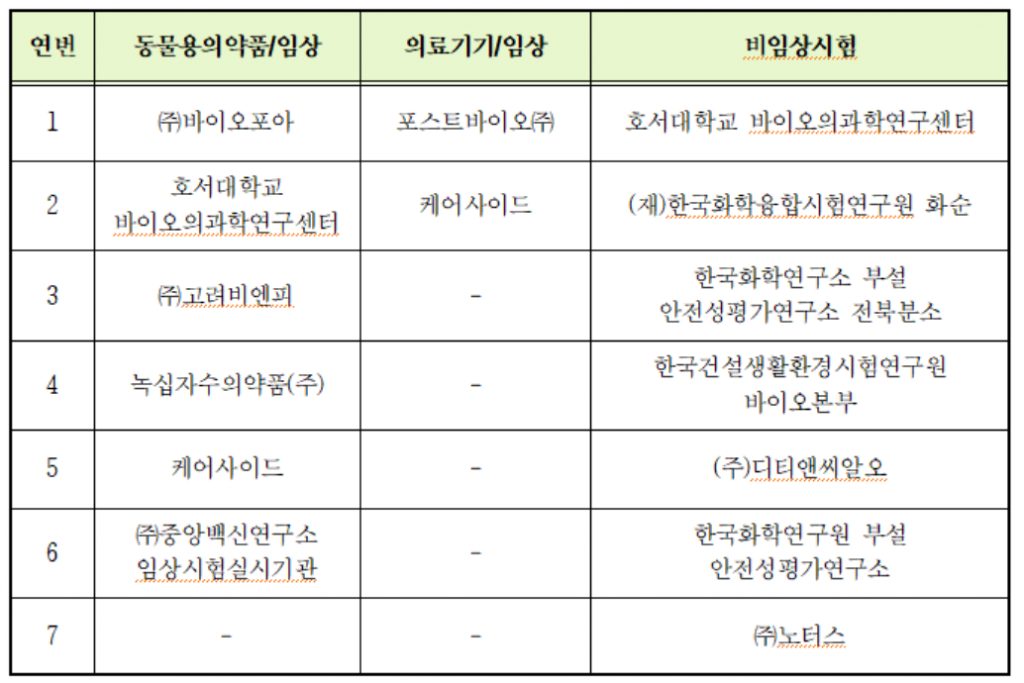 이에 따라 동물용의약품 임상 분야에선 (주)바이오포아 등 6곳, 의료기기 임상 분야에선 포스트바이오(주) 등 2곳, 그리고 비임상시험 분야에선 (주)노터스 등 7곳 등 모두 15곳의 시험실시기관을 선정 공표했다.
이에 따라 동물용의약품 임상 분야에선 (주)바이오포아 등 6곳, 의료기기 임상 분야에선 포스트바이오(주) 등 2곳, 그리고 비임상시험 분야에선 (주)노터스 등 7곳 등 모두 15곳의 시험실시기관을 선정 공표했다.
이들 15곳이 아닌, 다른 곳 시험결과는 인정하지 않는다는 얘기다.
그동안 동물용의약품 등 제조(수입) 품목허가를 내줄 때는 업체가 제출하는 안전성・유효성 심사자료는 대학 및 연구기관 등 국내외 전문기관에서 시험한 자료도 인정받았으나, 9월 15일부터는 독성시험 잔류성시험 소독제효력시험 등 핵심 심사자료의 경우 모두 이들 '지정' 시험실시기관에서 시험한 자료만 인정해주는 방식으로 바뀌기 때문이다.
하지만 21일 현재, 시험실시기관 선정을 신청한 곳이 29곳이 더 남아있어 시험 능력을 충분히 갖춘 몇 곳은 추가 선정될 가능성도 아직 남아있다.
검역본부는 "품목허가 심사자료의 객관성 및 신뢰성을 확보하기 위한 중요한 첫 걸음"이라 설명하고 "다만, 이 고시 시행 당시 종전의 규정에 따라 상기 시험을 실시하거나 시행 전에 임상시험 계획서를 제출한 품목에 대해서는 종전의 규정에 따르게 된다"고 덧붙였다.
한편, 세부 지정 내역은 농림축산검역본부 누리집 알림마당(www.qia.go.kr) -부서별 공지사항에서 확인할 수 있다.









